
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
چرا اسید 4-نیتروبنزوئیک اسید قوی تر از اسید بنزوئیک است؟
در شیمی آلی ، تغییرات ظریف در ساختار مولکولی می تواند منجر به تفاوت معنی داری در خواص شیمیایی شود. نمونه بارز تفاوت اسیدیته بین اسید بنزوئیک و اسید 4-نیتروبنزوئیک است. اما چه چیزی باعث می شوداسید 4 نیتروبنزوئیکیک اسید قوی تر؟ بیایید علم پشت این پدیده را کشف کنیم.
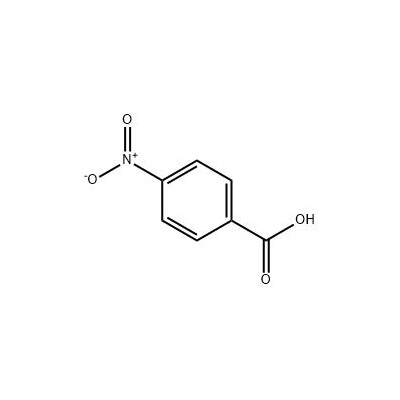
نقش ثبات پایه مزدوج
استحکام یک اسید تا حد زیادی با پایداری پایه کونژوگه آن تعیین می شود. هنگامی که یک اسید کربوکسیلیک (-COOH) یک پروتون (H⁺) را از دست می دهد ، یون کربوکسیلات (-coo⁻) را تشکیل می دهد. هرچه این یون با ثبات تر باشد ، اسید سریعتر پروتون خود را اهدا می کند و از این طریق اسیدیته خود را افزایش می دهد.
- اسید بنزوئیک: هنگامی که اسید بنزوئیک پروتون را از دست می دهد ، بار منفی بر روی دو اتم اکسیژن گروه کربوکسیلات جابجا می شود. حلقه معطر همچنین می تواند تا حدودی در حذف بار شارژ شرکت کند ، اما تأثیر آن متوسط است.
-اسید 4-نیتروبنزوئیک: در مقابل ، اسید 4-نیتروبنزوئیک دارای یک گروه نیترو (-NO₂) است که در موقعیت پارا نسبت به گروه کربوکسیل وصل شده است. گروه نیترو یک گروه قدرتمند با الکترونی است.
اثرات برداشت الکترون: تثبیت القایی و رزونانس
اثر استقرایی
گروه نیترو به دلیل الکترونگاتیو بودن اتم های اکسیژن آن ، اثر القایی شدیدی را اعمال می کند. این اثر چگالی الکترون را از حلقه معطر و گروه کربوکسیلات دور می کند و بار منفی را در پایه کونژوگه تثبیت می کند.
اثر تشدید
علاوه بر اثر القایی ، گروه نیترو همچنین می تواند پایه کونژوگه را از طریق طنین تثبیت کند. جابجایی بار منفی افزایش می یابد زیرا گروه نیترو امکان ساختارهای رزونانس اضافی را فراهم می کند. این فرم های رزونانس اضافی بیشتر بار را بر روی مولکول توزیع می کنند ، انرژی پایه کونژوگه را کاهش می دهند و باعث می شود که محرومیت مطلوب تر شود.
مقادیر PKA: تعیین اسیدیته
تفاوت در اسیدیته را می توان با مقایسه مقادیر PKA دو اسید اندازه گیری کرد:
- بنزوئیک اسید: دارای PKA تقریباً 4.2 است.
- اسید 4-نیتروبنزوئیک: دارای PKA در حدود 3.4 تا 3.5 است.
مقدار PKA پایین تر یک اسید قوی تر را نشان می دهد ، تأیید می کند که اسید 4-نیتروبنزوئیک در واقع اسیدی تر از اسید بنزوئیک است. کاهش تقریباً 0.8 تا 0.9 واحد در PKA در درجه اول به دلیل اثرات برداشت الکترون در گروه نیترو است.
پیامدها و برنامه های کاربردی
دانستن اینکه چرا اسید 4-نیتروبنزوئیک یک اسید قوی تر است ، فقط یک تمرین دانشگاهی نیست-این کاربردهای عملی در:
- سنتز: جایی که استحکام اسید بر مکانیسم های واکنش و نتایج تأثیر می گذارد.
- علم مواد: در طراحی ترکیبات با خصوصیات خاص اسید.
- شیمی دارویی: جایی که اسیدیته یک ترکیب می تواند بر فراهمی زیستی و تعامل آن با اهداف بیولوژیکی تأثیر بگذارد.
اسید 4 نیتروبنزوئیکیک اسید قوی تر از اسید بنزوئیک است زیرا گروه نیترو در موقعیت پارا به طور قابل توجهی پایه کونژوگه خود را تثبیت می کند. از طریق هر دو اثر القایی و رزونانس ، گروه نیترو به طور مؤثر بار منفی را پس از محرومیت کاهش می دهد و باعث می شود اسید مایل به اهدای پروتون باشد. این ثبات افزایش یافته به PKA پایین تر و افزایش اسیدیته تبدیل می شود.
دانستن این مفاهیم برای شیمیدانانی که مولکول ها را برای کاربردهای مختلف طراحی و دستکاری می کنند ، ضروری است و تأثیرات عمیقی را که جایگزین ها می توانند بر رفتار شیمیایی داشته باشند ، برجسته می کند. این که آیا شما دانشجویی هستید که به شیمی ارگانیک یا یک محقق فصلی می پردازید ، قدردانی از تعامل ظریف نیروهای مولکولی می تواند درک عمیق تری از واکنش و طراحی شیمیایی را باز کند.
Jiangsu Run'an Pharmaceutical Co. Ltd. یک شرکت تابعه کاملاً متعلق به Jiangsu Zhengda Qingjiang Pharmaceutical ، آموزشی ویبولیتین است. مواد اولیه ، و بازار بین المللی را باز کنید. این یک اقدام مهم برای تسریع در صنعتی شدن محصولات جدید و انجام برنامه ریزی استراتژیک بلند مدت است. وب سایت ما را درhttps://www.jsrapharm.com/برای اطلاعات بیشتر در مورد محصولات ما. اگر سوالی دارید ، در صورت تمایل با ما در wangjing@ctqjph.com تماس بگیرید.


